【疫苗競賽】歐美第二波難受控 只能揠「苗」助長? - 撰文:伍振中
【疫苗競賽】歐美第二波難受控 只能揠「苗」助長?
撰文:伍振中 2020-09-26 12:40
全球新冠肺炎疫情未曾消褪,歐洲、加拿大等地更迎來第二波疫情反彈。與此同時,各國在疫苗競速的戰場上愈趨白熱化。
各國政府及藥廠紛紛選擇「走捷徑」,規避一些非危及疫苗安全的常態行政程序及試驗方式,把握時間,冀有效疫苗能儘快推出市面──正值世紀大疫下的全球疫苗競賽,這是揠「苗」助長,還是回應大局的權宜之計?
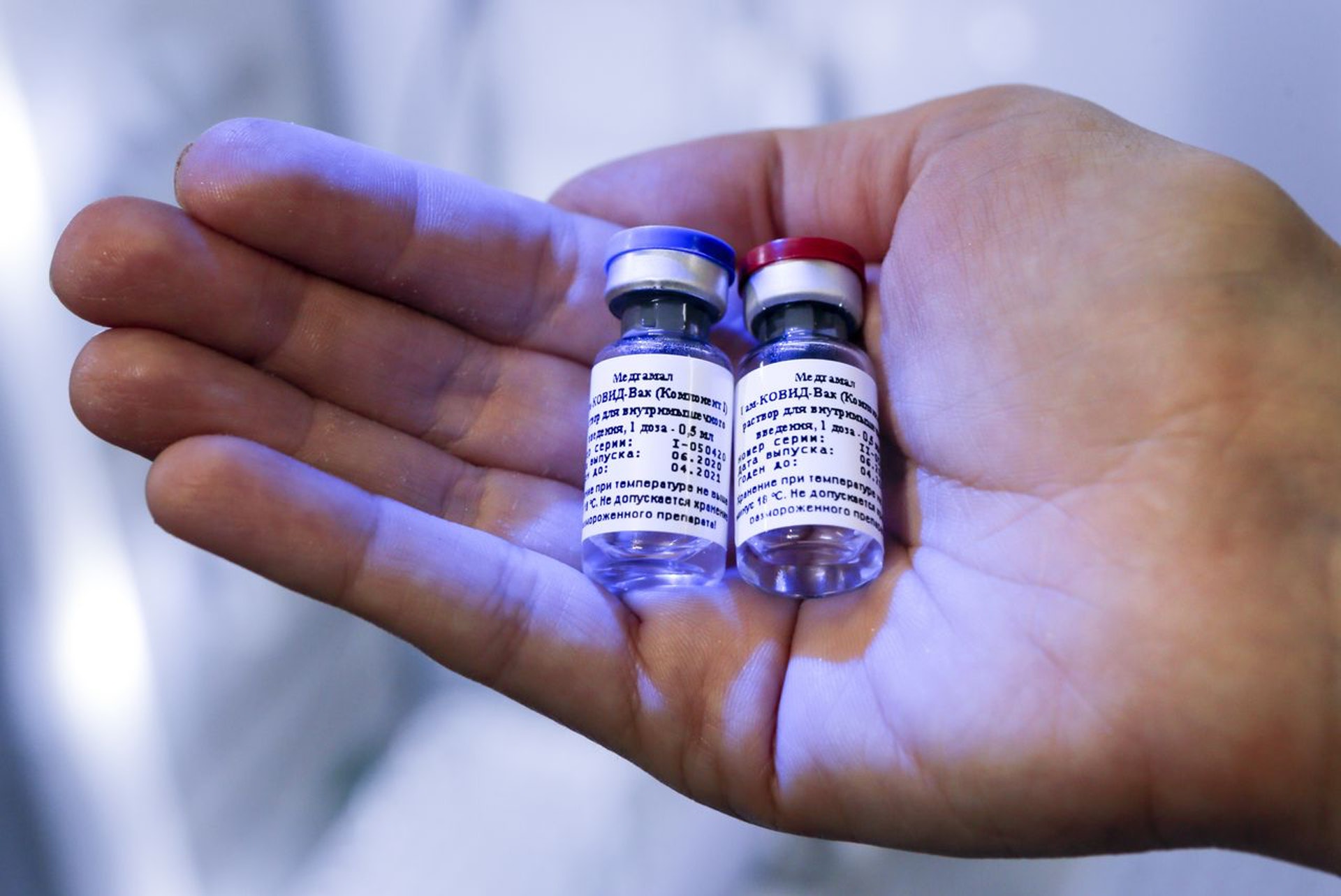
英國媒體本周三(23日)引述消息人士報道,英國計劃進行一項「人體挑戰試驗」(human challenge trial),用作測試候選新冠肺炎疫苗。這是針對新冠肺炎病毒的首項「人體挑戰試驗」計劃。
「人體挑戰試驗」即首先讓志願者接種候選新冠肺炎疫苗,然後人為地將新型冠狀病毒(SARS-CoV-2)當作挑戰標的,輸入志願者人體,以測試先前接種的疫苗對病毒有否產生免疫作用。這樣做的好處是能在短時間內擴大疫苗試驗樣本規模,令有效、安全的新冠肺炎疫苗能夠及早面世。據英國媒體報道,目前已有約2,000名志願者通過「人體挑戰試驗」倡議組織1Day Sooner報名參與計劃。英國政府對「人體挑戰試驗」亦開綠燈,撥款資助這項試驗計劃。
觀乎全球研發過程已進入第三階段的領跑候選疫苗,暫時普遍認為有八支。惟報道並沒有披露該「人體挑戰試驗」計劃將會選取哪些候選疫苗以作試驗之用。
「人體挑戰試驗」的應用最早可追溯至18世紀末,「疫苗之父」詹納(Edward Jenner)研發牛痘疫苗時曾經採用該試驗方式。觀乎近代醫學史,亦有醫學專家以此法協助研發傷寒、霍亂、瘧疾等疫苗。
「人體挑戰試驗」故意將病毒輸入人體,這不免涉及倫理道德之爭議。但適逢疫情遠未見完結之日,一支有效而安全的新冠肺炎疫苗急需面世以遏止疫情。於是,1Day Sooner發起聯署,倡議將「人體挑戰試驗」應用於新冠肺炎疫苗研發。
「當我們如今史無前例地面對新冠肺炎的全球威脅,實施一套受到嚴格控制的挑戰試驗,以冀研發並分辨出一個最佳疫苗,這是合乎道德規範。」牛津大學(Oxford University)醫學倫理學教授Dominic Wilkinson向英國媒體表示。他自己亦響應了1Day Sooner發起的聯署。
今次疫症波及全球,各國政府投入疫苗競速大賽。為求疫苗儘快面世,各國迫不得已採用不同「捷徑」開發疫苗,希望儘快遏止疫情。英國作為首個國家推出新冠肺炎「人體挑戰試驗」,只是其中一例。
心急如焚的特朗普
在美國,近月來社會上議論紛紛,猜測新冠肺炎疫苗究竟能否在11月3日總統大選前成功面世。特朗普多次向外界表示,疫苗將在10月內,即大選之前,推出市面。然而,白宮如此進取,卻讓外界擔心行政當局為儘快推出新冠肺炎疫苗,而犧牲應有的安全性和成效。
過往研發一支針對單一頑疾的疫苗,往往需要數年、甚至超過十年時間。如今各大藥廠集中火力,務求儘可能壓縮新冠肺炎疫苗的研發日程,經已省略了很多非必要的行政程序。但如白宮所願於數月內便能將有效疫苗推出市面,這真有可能嗎?

特朗普與正在向記者演說簡報的新白宮防疫顧問阿特拉斯(Scott Atlas),他們的抗疫主張相當一致。(AP)
早前美國媒體曾報道,美國食品和藥物管理局(FDA)或許會向有力候選疫苗批出「緊急使用授權」(Emergency Use Authorization,EUA),疫苗在大選前面世瞬現曙光。然而,《華盛頓郵報》日前卻報道,FDA最新推出的新冠肺炎疫苗EUA指引,將會提高批准門檻,計及檢視申請文件、最後階段臨床測試結果所需時間,估計很難有疫苗能趕及在11月前推出市面。
由於FDA最新指引要求最後階段臨床受試者的追蹤日數至少要達兩個月,所以儘管是輝瑞/BioNTech(BNT162b2)、莫德納(mRNA-1273)等已展開最後臨床試驗階段的疫苗,都相信難以在大選前面世。
然而,特朗普卻公開表示,可能會阻止FDA的新指引出台,更形容有關指引別具「政治化」。

圖為8月14日,一名實驗室員工在阿根廷的生物製藥公司mAbxience製作由牛津大學和阿斯利康製藥公司(AstraZeneca)開發的新型冠狀病毒肺炎疫苗。(AP)
「女兒試過了並無大礙」
這樣催促疫苗面世、表現得心急如焚的國家領袖,特朗普顯然不是孤例。
遠在俄羅斯,由莫斯科加馬列亞國家研究院(Gamaleya Research Institute)研發的「衛星V」(Sputnik V)疫苗未曾完成第三階段測試,便早在8月11日在俄羅斯衛生部註冊成功,成為全球首支註冊疫苗。
為求令國民及外界對俄製疫苗寄予信心,俄羅斯總統普京(Vladimir Putin)向外宣稱其女兒已接種該疫苗,雖然曾輕微發燒,但並無大礙,且成功產生抗體。普京更謂該疫苗已經可以大規模投入市場,計劃先讓國內高危群組人士接種。

普京同樣希望俄羅斯自主研發的新冠肺炎疫苗,能夠獲得外界廣泛肯定。(Getty Images)
在這場世界疫苗競賽中,各國政府及藥廠紛紛尋求快速讓新冠肺炎疫苗面世的「捷徑」。行政部門向科研機構、監察部門施壓,最後會否得來揠苗助長的反效果?
當每天染疫死亡人數不斷攀升之際,如何能夠壓縮疫苗研發日程,而不失安全性及應有成效?專業醫學團隊的群策群力固然重要,但官僚團隊通力輔佐、適時補位所發揮出來的協同效應,才是疫苗競賽中應有的健康加成作用;當權者更不能把疫苗開發進程,變成為自己「拉票」的政治工具。
六大疫苗種類:






世界衛生組織(WHO)9月25日證實,已與台灣簽署新型冠狀病毒肺炎(COVID-19)的COVAX全球疫苗機制。台灣衛福部長陳時中表示,預計10月初會付訂金,他強調不會選擇大陸製的新冠肺炎疫苗。
目前共159個國家或經濟體加入全球採購疫苗平台COVAX。
COVAX是新冠肺炎防治工具加速取得機制(Access to COVID-19 Tools Accelerator)之下負責疫苗的單位,由全球疫苗與預防注射聯盟(Global Alliance for Vaccines and Immunisation,GAVI)、流行病防範創新聯盟(Coalition for Epidemic Preparedness Innovations,CEPI)及世界衛生組織共同主導,旨在加速推動COVID-19疫苗的研發和生產,並確保世界各國可公平取得疫苗。
世衛總幹事高級顧問艾爾沃德表示,目前共159個國家或經濟體加入平台,包括並非世衛成員的台灣。世衛並正與大陸磋商,在疫苗供應平台中扮演的角色,大陸可能會為平台供應疫苗。
陳時中25日在立法院接受立委質詢時表示,9月18日已與COVAX簽約,預計10月初會付訂金。他表示,COVAX平台政治力干預不多,有信心獲得公平分配,且台灣也確定在COVAX平台上不選擇中國大陸製的新冠肺炎疫苗。
中央流行疫情指揮中心發言人莊人祥同日表示,傳染病防疫諮詢委員會7月已排定優先接種對象,優先順序和流感疫苗類似,包括醫事人員、65歲以上高齡者及50歲以上慢性病患者等,目標是讓全台60%人口、約1358萬人都能接種新冠肺炎疫苗。
莊人祥指出,COVAX合作主要分為2種方案,一是承諾採購,由COVAX分配疫苗,另一種則是選擇性採購,台灣9月18日已和COVAX簽約,並選擇「選擇性採購」方案,在疫苗選擇上有較大的主動權,但訂金、數量等詳細簽約內容,暫時不便多談。
莊人祥透露,整個簽約過程特別找了律師協助,但因部分內容還未定案,加上目前全球只有9支候選疫苗進入第三期臨床試驗,也都還沒有結果,疫苗安全性、有效性仍有待進一步證實及掌握。
至於台灣自身研發疫苗的進度,陳時中說,台灣有三家業者向衛福部申請新冠肺炎疫苗臨床試驗,都已獲通過,本周都會進入第一期臨床試驗,但具體狀況要看實驗反應,時間沒有辦法完全掌握。
大陸研發疫苗方面,科技部社會發展科技司司長吳遠彬25日指出,11款由中國大陸研發的新冠肺炎疫苗現時已進入臨床實驗階段,其中4款進入三期臨床試驗,預計新冠疫苗於今年年底年產能達6.1億劑,明年年產可達到10億劑以上。